药品生产质量管理规范GMP(多图,看这一篇就够)
《药品生产质量管理规范》(GMP)(1988年颁布,1998、2010年修订),规范中将无菌药品生产所需的洁净区ABCD等4个级别。
《药品生产质量管理规范》(GMP)(1988年颁布,1998、2010年修订),规范中将无菌药品生产所需的洁净区ABCD等4个级别。
A级:高风险操作区,如灌装区、放置胶塞桶和与无菌制剂直接接触的敞口包装容器的区域及无菌装配或连接操作的区域,应当用单向流操作台(罩)维持该区的环境状态。单向流系统在其工作区域必须均匀送风,风速为0.36-0.54m/s(指导值)。应当有数据证明单向流的状态并经过验证。在密闭的隔离操作器或手套箱内,可使用较低的风速。
B级:指无菌配制和灌装等高风险操作A级洁净区所处的背景区域。
C级和D级:指无菌药品生产过程中重要程度较低操作步骤的洁净区。
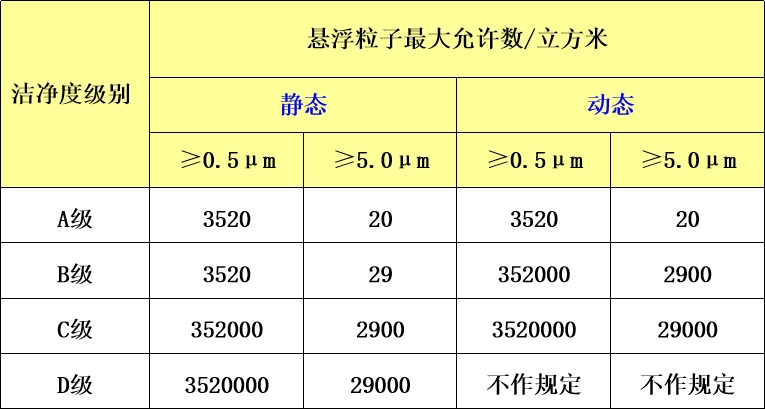
各级别空气悬浮粒子的标准
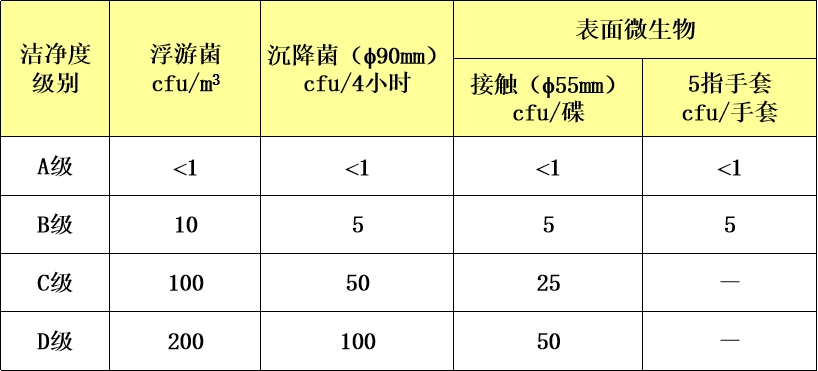
洁净区微生物监测的动态标准
注:菌落形成单位(CFU)是指在琼脂平板上经过一定温度和时间培养后形成的每一个菌落,是计算细菌或霉菌数目的单位。
最终灭菌药品的生产操作环境
非最终灭菌产品的生产操作环境
所谓无菌药品指的是法定药品标准中列有无菌检查项目的制剂和原料药,包括无菌制剂和无菌原料药。
非无菌药品:是指法定药品标准中未列无菌检查项目的制剂。
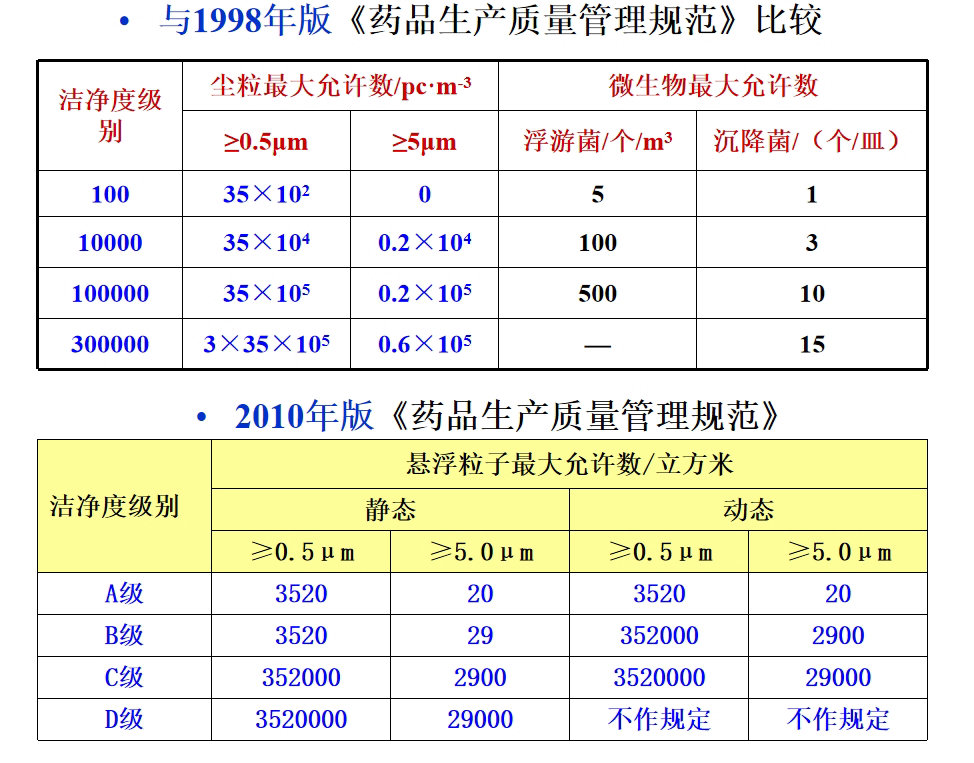
1998版的药品生产质量管理规范和2010年版本的对比如下:
本文版权归网站所有,转载请联系并注明出处:
http://www.ksqingyang.com/news-detail/NMwrjvZb